研究亮点
当前位置:首页 > 科学研究 > 研究亮点
上海光源生物大分子晶体学线站用户最新成果已在CELL正式发表
时间:2010-05-06
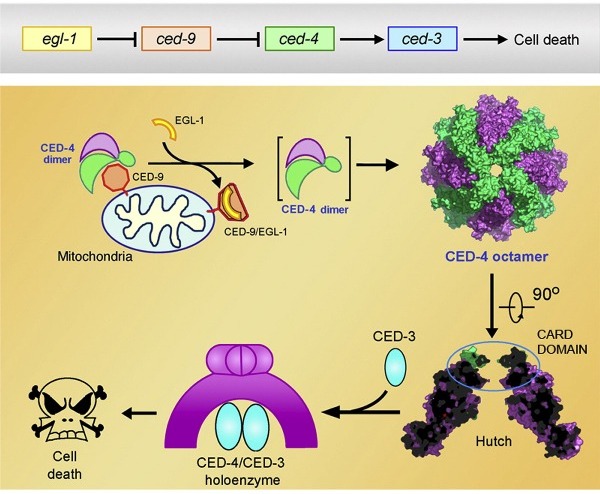
清华大学生命学院施一公、医学院颜宁研究组在CELL发表论文揭示CED-4细胞凋亡体的结构与功能机理。
施一公教授领导的实验室一直致力于对细胞凋亡调控机理的研究。颜宁教授的博士研究即因为揭示EGL-1、CED-9调控CED-4的机理而获得2005年的“青年科学家奖”(北美地区),这条通路上的下一个重要问题CED-4激活CED-3蛋白酶的分子机理一直不清楚。他们研究CED-4细胞凋亡体的结构与功能近10年,中间一度陷入瓶颈状态。直至2008年,在清华大学的实验室成功解析了CED-4的3.8埃的晶体结构。据知,这是施一公和颜宁回国之后解析的第一个重要结构,此后又历经十数次在美、日、中五个同步辐射的数据收集,终于利用在上海光源生物大分子晶体学线站收集的数据把结构修正到3.55埃,同时经过近两年的生化分析,初步揭示了CED-4调控CED-3的机理,研究结果于2010年4月30日发表于CELL(“Crystal Structure of the Caenorhabditis elegans Apoptosome Reveals an Octameric Assembly of CED-4”;Volume 141, Issue 3, 30 April 2010, Pages 446-457)。
他们的工作显示CED-4细胞凋亡体以八聚体的形式存在。CED-4八聚体组成一个碗状结构。他们还解析了CED-4与CED-3的复合物结构,然而,尽管晶体中确实含有CED-3,结构中却看不到CED-3的存在。晶体学分析显示CED-3坐落于CED-4的碗中,其衍射密度因不对称性而抵消。基于结构和生化实验结果,他们提出了CED-4激活CED-3的分子机制模型:CED-4八聚体通过募集两个CED-3分子到它的碗中而激活CED-3,CED-4的存在提高了CED-3的蛋白水解酶的活性,而执行其杀死细胞的功能。同时,CED-4作为AAA+ ATPase家族的重要成员,该结构显示了与以往不同的AAA+ ATPase寡聚化形式,并揭示了NB-ARC(nucleotide-binding, Apaf-1,R proteins, and CED-4)家族蛋白结构组织上的一些共同原则,为研究这一家族的植物抗性R蛋白以及发炎体(inflammasome)的结构与功能提供了重要基础。
细胞凋亡(程序性细胞死亡)是在所有多细胞生物中起关键作用的基本生命过程,细胞凋亡的异常会导致严重病变,比如癌症、老年痴呆症等等。因此揭示细胞凋亡的分子机理不仅可以加深我们对这一基本生命过程的了解,还可以对开发新型抗癌、预防老年痴呆的药物起提供线索。
研究细胞凋亡的一个重要模式生物是秀丽线虫(Caenorhabditis elegans),MIT的Bob Horvitz教授领导的研究组因为通过遗传学揭示egl-1,ced-9,ced-4和ced-3 组成的程序性细胞死亡的线性调控通路而获得2002年的诺贝尔奖。
Cell简介:
出版方:美国Cell Press(隶属爱思唯尔Elsevier出版集团)
影响因子:31.253 (2008)。
创刊:1976年
刊期:双周刊,尚无中文版
定位:Cell是与《Science》、《Nature》等齐名的世界权威杂志,是生命科学研究领域的顶尖杂志。创刊30多年间,Cell出版社旗下期刊共发表了59篇诺贝尔奖获得者的论文,其中10篇论文为作者的获奖论文。据2003年6月Thomson ISI 最新统计数据表明,Cell是近10年来在分子生物学和遗传学研究领域中最热门和最具影响力的期刊。