上海光源生物大分子晶体学线站用户在CRISPR-Cas系统切割RNA研究中取得重大进展
2017年7月27日,《细胞》(Cell)杂志在线发表了中国科学院生物物理研究所王艳丽课题组和章新政课题组在VI型CRISPR-Cas系统效应蛋白Cas13a(亦称C2c2)结构研究中取得的新进展,论文题目为“The Molecular Architecture for RNA-Guided RNA Cleavage by Cas13a”。该研究证实target RNA的结合导致LbuCas13a的两个HEPN(发挥RNA干扰功能的结构域)结构域发生构象变化,从而激发LbuCas13a非特异性地切割任意单链RNA的酶切活性,该成果为研究Cas13a发挥RNA酶活性的分子机制提供了重要的结构生物学基础。
几乎所有的古菌和约50%的细菌都具有CRISPR-Cas系统,用以抵抗病毒和质粒的侵染。CRISPR-Cas系统分为两大类,Cas13a是第二大类VI型系统中的效应蛋白,具有RNA介导的RNA酶切活性,是目前第二大类CRISPR-Cas系统发现的唯一能够降解RNA的蛋白(Cas9,Cpf1,C2c1均是RNA介导的DNA核酸内切酶),对开发研究RNA工具,扩展CRISPR系统在基因编辑方面的运用具有重大价值。
在该研究中,研究人员利用上海光源生物大分子晶体学线站(BL17U1)成功解析了LbuCas13a-crRNA-target RNA的三元复合物结构(3.08Å),并通过冷冻电镜技术,获得了3.2Å LbuCas13a-crRNA的二元复合物结构。结构显示Cas13a具有REC和NUC两个叶片,其中NUC叶片包含两个HEPN结构域、Helical-2结构域以及连接两个HEPN结构域的连接结构域,两个HEPN结构域组成了Cas13a切割target RNA的活性区域。crRNA识别序列互补的目的RNA,并与之结合形成双链RNA并被NUC叶片包围。同时,双链RNA的形成引起crRNA和Cas13a蛋白的构象变化,促使两个HEPN结构域相互靠近,进而激活Cas13a蛋白。研究人员通过结构和功能证明由crRNA和target RNA激活的Cas13a能切割任意单链的RNA。该研究发现为CRISPR-Cas13a系统的进一步开发提供了可靠的结构基础,对深入理解细菌抵御病毒入侵的分子机制提供了强有力的证据,并将对病毒引起的疾病的预防、检测、控制与治疗产生重大意义,特别是基于Cas13a高效的RNA酶切活性,对其应用于各类重大疾病的快速检测具有十分广阔的前景。(生命科学研究部 供稿)
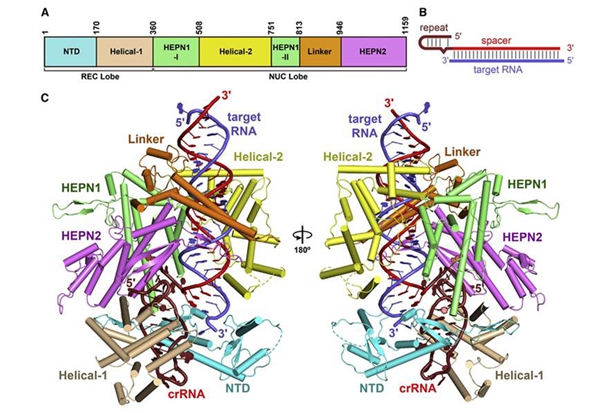
LbuCas13a-crRNA-target RNA三元复合物的晶体结构
全文链接:http://www.cell.com/cell/fulltext/S0092-8674(17)30769-9
附件下载:
